Химические свойства воды
Если в цилиндр с водой опустить стружки кальция, то от поверхности кальция начнут отрываться пузырьки газа, как от поверхности цинка, помещенного в раствор серной кислоты. При поднесении зажженной лучинки к отверстию цилиндра мы будем наблюдать вспышки. Это горит водород. Вода в цилиндре мутнеет. Появившиеся в цилиндре белые взвешенные частицы — гидроксид кальция Са(ОН)2. Протекающая реакция выражается уравнением:
Са + 2Н20 = 2Са (ОН)2 + Н2 ↑
 При этой реакции из молекулы воды Н2О, которую можно представить как Н—ОН (группа — ОН — гидроксогруппа), —ОН переходит в состав гидроксида кальция. Так как атом кальция двухвалентен, то он вытесняет из двух молекул воды два атома водорода, а оставшиеся две группы —ОН соединяются с атомом кальция.
При этой реакции из молекулы воды Н2О, которую можно представить как Н—ОН (группа — ОН — гидроксогруппа), —ОН переходит в состав гидроксида кальция. Так как атом кальция двухвалентен, то он вытесняет из двух молекул воды два атома водорода, а оставшиеся две группы —ОН соединяются с атомом кальция.
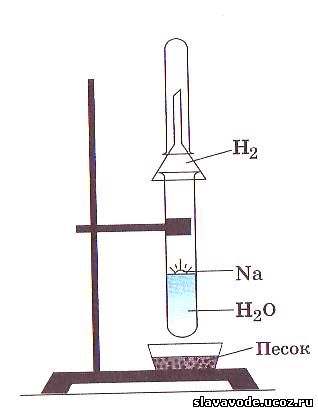
Еще энергичнее протекает реакция натрия с водой. Опустим кусочек натрия в стакан с водой. Натрий всплывает на ее поверхность, плавится, превращаясь в блестящую каплю. Она быстро перемещается по поверхности воды, издавая шипение и уменьшаясь в размерах. Выпарив раствор, мы обнаружим твердое белое вещество — гидроксид натрия NaOH
2Na + 2НОН = 2NaOH + Н2 ↑
Натрий и кальций принадлежат к числу наиболее химически активных.
Сожжем в банке на ложечке красный фосфор. Прильем немного воды и подождем, пока получившийся оксид фосфора (V) Р205 растворится. Добавим к раствору несколько капель фиолетового лакмуса. Лакмус окрасится в красный цвет. Значит, в растворе содержится кислота. Оксид фосфора (V) соединяется с водой, и получается фосфорная кислота Н3Р04:
Р205 + ЗН20 = 2Н3Р04
Сожжем в банке, в которую налито немного воды, серу и получившийся раствор исследуем раствором лакмуса. Он тоже окрасится в красный цвет. Оксид серы (IV) S02, образовавшийся при сгорании серы, соединился с водой, и получилась сернистая кислота:
S02 + H20 = H2S02
Оксид серы (VI), взаимодействуя с водой, образует серную кислоту H2S04:
SO 2 + Н2О = H2S04
Азот может образовать оксид N205, при взаимодействии которого с водой образуется азотная кислота:
N205 + Н20 = 2HN03
Соединения оксидов неметаллов с водой относят к кислотам.
 Рассмотрим теперь отношение к воде оксидов металлов. Насыплем в стаканчики оксид меди СиО, оксид железа Fe203, оксид цинка ZnO и оксид кальция СаО и прильем в каждый немного воды. Оксиды меди, железа и цинка в воде не растворяются и не соединяются с ней. Иначе ведет себя оксид кальция, или негашеная известь.
Рассмотрим теперь отношение к воде оксидов металлов. Насыплем в стаканчики оксид меди СиО, оксид железа Fe203, оксид цинка ZnO и оксид кальция СаО и прильем в каждый немного воды. Оксиды меди, железа и цинка в воде не растворяются и не соединяются с ней. Иначе ведет себя оксид кальция, или негашеная известь.
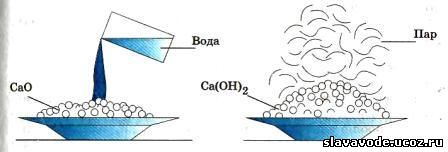
При обливании кусков негашеной извести водой наблюдается такое сильное разогревание, что часть воды превращается в пар, а куски негашеной извести, рассыпаясь, превращаются в сухой рыхлый порошок — гашеную известь, или гидроксид кальция Ca(OH)2 :
СаО + Н20 = Са(ОН)2
Подобно оксиду кальция, соединяются с водой оксиды натрия и калия:
Na20 + H20 = 2NaOH
К20+Н20 = 2КОН
При этих реакциях образуются гидроксид натрия NaOH и гидроксид калия КОН.
Таким образом, одни оксиды металлов не реагируют с водой (их большинство) другие (оксид калия, оксид натрия, оксид кальция, оксид бария и др.) соединяются с ней, образуя гидроксиды, которые относятся к основаниям.
(Неорганическая химия 7-8 класс автор Ю. В. Ходаков и др.)





